Введение
Это единения, содержащие карбонильную группу = С = О . У альдегидов карбонил связан радикалом и водородом. Общая формула альдегидов:
 R – C = O R – C = O
H
У кетонов карбонил связан с двумя радикалами. Общая формула кетонов:
 R1
– C = O R1
– C = O
R2
Альдегиды являются более активными, чем кетоны (у кетонов карбонил как бы блокирован радикалами с обеих сторон).
Классификация
1.по углеводородному радикалу (предельные, непредельные, ароматические, циклические).
2.по числу карбонильных групп (одна, две и тд.)
Изомерия и номенклатура
Изомерия альдегидов обусловлена изомерией углеродного скелета. У кетонов помимо изомерии углеродного скелета наблюдается изомерия положения карбонильной группы. По тривиальной номенклатуре альдегиды называют соответственно карбоновым кислотам, в которые они переходят при окислении. По научной номенклатуре названия альдегидов складываются из названий соответствующих углеводородов с добавлением окончания аль. Атом углерода альдегидной группы определяет начало нумерации. По эмпирической номенклатуре кетон называют по радикалам, связанным с карбоксилом с добавлением слова кетон. По научной номенклатуре названия кетонов складываются из названий соответствующих углеводородов с добавлением окончания ОН, в конце ставят номер углеродного атома, при котором стоит карбонил. Нумерацию начинают от ближайшего к кетонной группе конца цепи.
 Представители предельных альдегидов. Cn
H2
n
+1
C=O Представители предельных альдегидов. Cn
H2
n
+1
C=O
H
| Формула |
Тривиальное название |
Научное название |
 Н – С = О Н – С = О
Н
|
Муравьиный
Формальдегид
|
метаналь |
 СН3 – С = О СН3 – С = О
Н
|
Уксусный
Ацетальдегид
|
Этаналь |
 СН3 – СН2 – С = О СН3 – СН2 – С = О
Н
|
Пропионовый |
Пропаналь |
 СН3 – СН2 – СН2 – С = О СН3 – СН2 – СН2 – С = О
Н
|
Масляный
|
Бутаналь
|
 СН3 – (СН2)3 – С = О СН3 – (СН2)3 – С = О
Н
|
Валериановый
|
Пентаналь |
 СН3 – (СН2)4 – С = О СН3 – (СН2)4 – С = О
Н
|
Капроновый
|
Гексаналь |
Представители предельных кетонов
| Формула |
Эмпирическое название |
Научное название |
 СН3 – С = О СН3 – С = О
СН3
|
Диметилкетон |
Пропанон |
 СН3 – С = О СН3 – С = О
СН2 – СН3
|
Метилэтилкетон |
Бутенон |
 СН3 – С = О СН3 – С = О
СН2 – СН2 – СН3
|
Метилпропилкетон |
Пентанон -2 |
 СН3 – СН2 – С = О СН3 – СН2 – С = О
СН2 – СН3
|
Диэтилкетон |
Пентанон -3 |
 СН3 – С = О СН3 – С = О
 СН – СН3 СН – СН3
СН3
|
метилпропилкетон |
3-метилбутанон-2 |
Способы получения
1) Путем окисления спиртов. Из первичных спиртов получаются альдегиды, из вторичных кетоны. Окисление спиртов происходит при действии сильных окислителей (хромовая смесь) при небольшом нагревании. В промышленности в качестве окисления используют кислород воздуха в присутствии катализатора – меди (Cu) при t0
= 300-5000
С
  СН3
– СН2
– СН2
– ОН + О К2
Cr
2
O
7
CH3
– CH2
– C =O+ HOH СН3
– СН2
– СН2
– ОН + О К2
Cr
2
O
7
CH3
– CH2
– C =O+ HOH
пропанол -1 H
пропаналь
   СН3
– СН – СН3
+ О К2
Cr
2
O
7
СН3
– С – СН3 СН3
– СН – СН3
+ О К2
Cr
2
O
7
СН3
– С – СН3
ОН О
пропанол -2 пропанон
2) Термическое разложение кальциевых солей карбоновых кислот, причем, если взть соль муравьиной кислоты, то образуются альдегиды, а если других кислот, то кетоны.
 СН3
– С = О СН3
– С = О
    О – Са прокаливание СаСО3
+ СН3
– С = О О – Са прокаливание СаСО3
+ СН3
– С = О
 Н –С – О Н Н –С – О Н
О уксусный альдегид
 СН3
– С = О СН3
– С = О
    О – Са прокаливание СаСО3
+ СН3
– С = О О – Са прокаливание СаСО3
+ СН3
– С = О
 СН3
–С – О СН3 СН3
–С – О СН3
О ацетон
Это лабораторные способы получения.
3) По реакции Кучерова (из алкинов и воды, катализатор – соли ртути в кислой среде). Из ацетилена образуются альдегиды, из любых других алкинов – кетоны.
  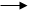  СН = СН + НОН СН2
= СН – ОН СН3
– С = О СН = СН + НОН СН2
= СН – ОН СН3
– С = О
ацетилен виниловый СН3
спирт уксусный альдегид
     СН3
– С = СН + НОН СН3
– С = СН2
СН3
– С = О СН3
– С = СН + НОН СН3
– С = СН2
СН3
– С = О
пропин ОН СН3
пропенол – 2 ацетон
4) Оксосинтез. Это прямое взаимодействие алкенов с водным газом (СО+Н2
) в присутствии кобальтового или никелевого катализаторов под давлением 100- 200 атмосфер при t0
= 100-2000
С. По этому способу получают альдегиды
   СН3
– СН2
– СН2
– С = О СН3
– СН2
– СН2
– С = О
бутаналь Н
 СН3
– СН = СН2
+ СО + Н2 СН3
– СН = СН2
+ СО + Н2
   СН3
– СН – С = О СН3
– СН – С = О
СН3
Н
2-метилпропаналь
5) Гидролиз дигалогенпроизводных. Если оба галогена находятся при первичном углеродном атоме, то образуется альдегид, если при вторичном – кетон.
   СН3
– СН2
– С – CL2
+ HOH 2HCL + CH3
– CH2
– C = O СН3
– СН2
– С – CL2
+ HOH 2HCL + CH3
– CH2
– C = O
H H
1,1-дихлорпропенпропеналь
 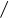   СН3
– С – CH3
+ HOH 2HCL + CH3
– C = O СН3
– С – CH3
+ HOH 2HCL + CH3
– C = O
CLCLCH3
2,2-дихлорпропан пропанон
Муравьиный альдегид – газ, другие низшие альдегиды и кетоны – жидкости, легко растворимые в воде; альдегиды обладают удушливым запахом, который при сильном разведении становится приятным(цветочным или фруктовым). Кетоны пахнут довольно приятно. Следовательно карбонил = С =О носитель запаха, поэтому альдегиды и кетоны применяются в парфюмерной промышленности. температура кипения альдегидов и кетонов возрастает по мере увеличения молекулярного веса.
Природа карбонильной группы
 Большинство реакций альдегидов и кетонов обусловлено присутствием карбонильной группы. рассмотрим природу карбонила = С =О. например, Большинство реакций альдегидов и кетонов обусловлено присутствием карбонильной группы. рассмотрим природу карбонила = С =О. например,
 R – C = O R – C = O
H
1.углерод с кислородом в карбониле связаны двойной связью : одна сигма - связь, другая пи – связь. За счет разрыва П- связи у альдегидов и кетонов идут реакции присоединения (нуклеофильного типа):
  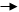 R – C = OR – C – O : R – C = OR – C – O :
HH
Кислород является более электроотрицательным элементом, чем углерод, и поэтому электронная плотность у атома кислорода больше, чем у атома углерода. При реакциях присоединения к углероду будет присоединяться нуклеофильная часть реагента, к кислороду – электрофильная часть.
2.приреакциях замещения может замещаться кислород карбонила. При этом происходит разрыв двойной связи между С и О
3.карбонил влияет на связи С – Н в радикале, ослабляя их, особенно в альфа-положении, то есть рядом с карбонильной группой.
   Н Н Н Н Н Н
    Н – α
С –β
С – γ
С – С = О Н – α
С –β
С – γ
С – С = О
Н Н Н Н
При действии свободных галогенов будет замещаться водород в углеродном радикале при альфа- углеродном атоме.
    СН3
– СН2
– СН2
– С = О + СL2
CH3
– CH2
– CH – C = O + HCL СН3
– СН2
– СН2
– С = О + СL2
CH3
– CH2
– CH – C = O + HCL
ОН CLOH
α–хлормасляный альдегид
Химические свойства
Из всех классов органических соединений альдегиды и кетоны самые реакционноспособные. Причем в химическом отношении альдегиды более активны, чем кетоны. Для них характерны следующие реакции: окисления, присоединения, замещения, полимеризации, конденсации. Для кетонов не характерны реакции полимеризации.
Реакции окисления
Альдегиды окисляются легко, даже слабыми окислителями HBrO, [Ag(NH3
)2
]OH, раствор Фелинга. При окислении альдегидов образуются карбоновые кислоты.
   СН3
– С = О + О СН3
– С = О – уксусная кислота СН3
– С = О + О СН3
– С = О – уксусная кислота
Н ОН
Если окислителем является [Ag(NH3
)2
]OH , то выделяется свободное серебро (реакция «серебряного зеркала» - это качественная реакция на альдегиды).
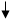    СН3
– С = О + 2[Ag(NH3
)2
]OH СН3
– С = О + 2 Ag + 4 NH3
+ Н2
О СН3
– С = О + 2[Ag(NH3
)2
]OH СН3
– С = О + 2 Ag + 4 NH3
+ Н2
О
Н ОН
Окисление кетонов происходит гораздо труднее и только сильными окислителями. Продуктами окисления являются карбоновые кислоты. При окислении кетона образуется спиртокетон, затем дикетон, который, разрываясь, образует кислоты.
 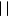 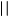    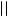   СН3
– СН2
– С – СН2
– СН3
+ О
СН3
– СН – С – СН2
– СН -Н2О
+О
СН3
– С – С – СН2
– СН3
+О +Н2О СН3
– СН2
– С – СН2
– СН3
+ О
СН3
– СН – С – СН2
– СН -Н2О
+О
СН3
– С – С – СН2
– СН3
+О +Н2О
О ОН О О О
диэтилкетон спиртокетон дикетон
   СН3
– С = О + О = С – СН2
– СН3 СН3
– С = О + О = С – СН2
– СН3
ОН ОН
уксусная к-та пропионовая к-та
В случае смешанного кетона окисление протекает по правилу Попова – Вагнера, то есть главное направление реакции – окисление соседнего с карбонилом наименее гидрированного атома углерода. Но помимо с главным направлением будет и побочное направление реакции, то есть окислится углеродный атом с другой стороны карбонила. При этом образуется смесь различных карбоновых кислот.
      СН3
– С – СН – СН3
– спиртокетон +О - Н2
О СН3
– С – СН – СН3
– спиртокетон +О - Н2
О
О ОН
      СН3
– С – СН2
– СН3
ОН О СН3
– С – СН2
– СН3
ОН О
  О СН2
– С – СН2
– СН3
+ О – Н2
О О СН2
– С – СН2
– СН3
+ О – Н2
О
Бутанон-2 спиртокетон
       СН3
– С – С – СН3
+О +Н2О
2 СН3
– С = О СН3
– С – С – СН3
+О +Н2О
2 СН3
– С = О
О О ОН
дикетон уксусная кислота
        СН–С – СН2
– СН3
+ О +Н2О
НС = О + СН3
– СН2
– С = О СН–С – СН2
– СН3
+ О +Н2О
НС = О + СН3
– СН2
– С = О
О О ОН ОН
дикетон муравьиная к-та пропионовая к-та
Реакции присоединения
Протекают за счет разрыва пи-связи в карбониле. Эти реакции нуклеофильного присоединения, то есть сначала к положительно заряженному углероду карбонила присоединяется нуклеофильная часть реагента со свободной электронной парой (протекает медленно):
  = С+
= О -
+ :Х -
= С – О – = С+
= О -
+ :Х -
= С – О –
Х
Вторая стадия – присоединение протона или другого катиона к образовавшемуся аниону (протекает быстро):
   = С – О –
+ Н +
= С – ОН = С – О –
+ Н +
= С – ОН
Х Х
1.Присоединение водорода.
При этом из альдегидов получаются первичные спирты, из кетонов – вторичные. Реакция протекает в присутствии катализаторов Ni, Pt и др.
  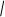  СН3
– С = О + Н +
: Н -
СН3
– С – Н СН3
– С = О + Н +
: Н -
СН3
– С – Н
ОН Н ОН
уксусный альдегид этанол
    СН3
– С – СН3
+ Н+
: Н -
СН3
– СН – СН3 СН3
– С – СН3
+ Н+
: Н -
СН3
– СН – СН3
О ОН
пропанон пропанол -2
2.Присоединение бисульфата натрия (гидросульфата):
    R – C = O + HSO3
Na R – C – SO3
Na R – C = O + HSO3
Na R – C – SO3
Na
HOHH
При этом образуются бисульфитные производные. Эту реакцию используют для очистки альдегидов и кетонов и выделения их из примесей.
3.Присоединение синильной кислоты. При этом образуются α- оксинитрилы, которые являются промежуточными продуктами синтеза оксикислот, аминокислот:
 OH OH
    R – C = O + HCNR – C – C=N R – C = O + HCNR – C – C=N
HH
α- оксинитрил
4. Присоединение аммиака NH3
. При этом образуются оксиамины.
   R – C = O + H – NH2
CH3
– CH – NH2 R – C = O + H – NH2
CH3
– CH – NH2
HOH
Оксиамин
5. Присоединение магнийгалогенорганических соединений (реактив Гриньяра). Реакцию используют для получения спиртов.
6.Присоединение спиртов (безводных). При этом первоначально образуются полуацетали (как обычная реакция присоединения). Затем при нагревании с избытком спирта образуются ацетали (как простые эфиры).
     R – C = O + СН3
– ОН R – CН – О – СН3
+СН3ОН R – C = O + СН3
– ОН R – CН – О – СН3
+СН3ОН
 R – CН – О – СН3 R – CН – О – СН3
HОН О – СН3
полуацеталь ацеталь
В природе очень много соединений полуацетального и ацетального характера, особенно среди углеводов (сахаров).
Реакции замещения
Кислород карбонильных групп может замещаться на галогены и некоторые азотсодержащие соединения.
1.Замещение галогенами. Происходит при действии на альдегиды и кетоны фосфорных соединений галогенов PCL3
и PCL5
. При действии же свободными галогенами замещается водород в углеводородном радикале при α-углеродном атоме.
  + PCL5
CH3
– CH2
– CH –CL2
+ POCL3 + PCL5
CH3
– CH2
– CH –CL2
+ POCL3
  СН3
– СН2
– С = О 1,1-дихлорпопин (фосфора хлорокись) СН3
– СН2
– С = О 1,1-дихлорпопин (фосфора хлорокись)
  Н +CL2
CH3
– CH – CH = O + HCL Н +CL2
CH3
– CH – CH = O + HCL
пропаналь CL
α-монохлорпропионовый альдегид
2.Реакция с гидроксиамином NH2
OH. При этом образуются окислы альдегидов (альдоксилы) и кетонов (кетоксины).
 СН3
– СН = О + Н2
N – OHCH3
– CH – N – OH+ H2
O СН3
– СН = О + Н2
N – OHCH3
– CH – N – OH+ H2
O
уксусный альдегид оксиэтаналь
Эту реакцию применяют для количественного определения карбоксильных соединений.
3.Реакция с гидразином NH2
– NH2
. Продуктами реакции являются гидразины (когда реагирует одна молекула альдегида или кетона) и азины (когда реагируют две молекулы).
 СН3
– СН = О + NH2
– NH2
СН3
– СН = N – NH2 СН3
– СН = О + NH2
– NH2
СН3
– СН = N – NH2
этаналь гидразин гидразин этаналь
 СН3
– СН = N – NH2
+ О = СН – СН3
СН3
– СН =N – N = НС – СН3 СН3
– СН = N – NH2
+ О = СН – СН3
СН3
– СН =N – N = НС – СН3
азин этаналь (альдазин)
4.Реакции с фенилгидразином. С6
Н5
– NH – NH2
. Продуктами реакции являются фенилгидразины.
 СН3
– СН = О + Н2
N – NH – C6
H5
CH3
– CH = N – NH – C6
H5 СН3
– СН = О + Н2
N – NH – C6
H5
CH3
– CH = N – NH – C6
H5
Фенилгидразонэтаналь
Окислы, гидразины, азины, фенилгидразины – твердые кристаллические вещества с характерными температурами плавления, по которым определяют природу (строение) карбонильного соединения.
Реакции полимеризации
Характерны только для альдегидов. Но и то, только газообразные и летучие альдегиды (муравьиный, уксусный) подвергаются полимеризации. Это очень удобно при хранении этих альдегидов. муравьиный альдегид полимеризуется в присутствии серной кислоты или соляной, при нормальной температуре. Коэффициент полимеризации n=10-50. Продукт полимеризации – твердое вещество, называется – полиоксиметилен (формалин).
        Н Н Н Н Н Н Н Н
       Н – С = О – С – О – С – О – ...– С – … – С – О – Н – С = О – С – О – С – О – ...– С – … – С – О –
  Н Н Н Н Н n Н Н Н Н Н n
Полиоксиметилен
Это твердое вещество, но его можно превратить в муравьиный альдегид, разбавляя водой и слегка подогревая.
Уксусный альдегид под влиянием кислот образует жидкий циклический триммер- паральдозу и твердый тетрамер – метальдозу («сухой спирт»).
  3 СН3
– СН = О О 3 СН3
– СН = О О
СН3
- НС СН – СН3
О О
СН – СН3
паральдегид
    4 СН3
– СН = О СН3
– НС О 4 СН3
– СН = О СН3
– НС О
  О СН – СН3 О СН – СН3
  СН5
– НС О СН5
– НС О
 О СН – СН3 О СН – СН3
Метальдегид
Реакции конденсации
1.Альдегиды в слабо основной среде (в присутствии ацетона калия, поташа, сульфата калия) подвергаются альдольной конденсации с образованием альдегидо - спиртов, сокращенно называемых альдолями. Разработана эта реакция химиком А.П. Бородиным (он же композитор). В реакции участвует одна молекула своей карбонильной группой, а другая молекула водородом при α- углеродном атоме.
  СН3
– СН = О + НСН2
– СН = О СН3
– СН – СН2
– СН = О СН3
– СН = О + НСН2
– СН = О СН3
– СН – СН2
– СН = О
ОН альдоль
(3 – оксибутаналь или β-оксимасляный альдегид)
    СН3
– СН – СН2
– СН = О + НСН2
– СН = О СН3
– СН – СН2
– СН – СН2
–СН =О СН3
– СН – СН2
– СН = О + НСН2
– СН = О СН3
– СН – СН2
– СН – СН2
–СН =О
ОН ОН ОН
гексенциол-3,5-аль
С каждым разом увеличивается число групп ОН. Получается альдегидная смола при уплотнении большого числа молекул.
2. Кротоновая конденсация . для альдегидов она является продолжением альдольной конденсации, то есть при нагревании альдоль отщепляет воду с образованием непредельного альдегида.
   СН3
– СН – СН2
– СН = О СН3
– СН = СН – С = О СН3
– СН – СН2
– СН = О СН3
– СН = СН – С = О
ОН ОН
кротоновый альдегид
Рассмотрим эти реакции для кетонов.
         СН3
– С = О + НСН2
– С = О СН3
– С – СН2
– С = О СН3
– С = СН – С = О СН3
– С = О + НСН2
– С = О СН3
– С – СН2
– С = О СН3
– С = СН – С = О
СН3
СН3
ОН СН3
СН3
СН3
СН3
4 – окси – 4 – метилпентанон-2 4 – метилпентан -3-он-2
3.Сложноэфирная конденсация. Характерна только для альдегидов. Разработана В.Е.Тищенко. протекает в присутствии катализаторов алкоголятов алюминия (CH3
– CH2
– O)3
AL.
  CH3
– CH = O + O = HC – CH3
CH3
– СН2
– О – С = О CH3
– CH = O + O = HC – CH3
CH3
– СН2
– О – С = О
СН3
уксусноэтиловый эфир
Они содержат в углеводородном радикале двойную связь. Представители:
1.СН2
= СН – СН =О – пропен-2-аль - акриловый альдегид или акролеин
2.СН3
– СН = СН – СН = О – бутен – 2 – аль - кротоновый альдегид
Акролеин иначе называют чад, он получается при нагревании горении жиров. В химическом отношении непредельные альдегиды обладают всеми свойствами предельных по карбонильной группе, а за счет двойной связи в радикале могут вступать в реакции присоединения.
У этих альдегидов сопряженная система двойных связей, поэтому в химическом отношении они отличаются реакциями присоединения. Присоединение водорода, галогенов, галогенводородов происходит по концам сопряженной системы.
Электронная плотность смещена к кислороду и к нему направляются положительно заряженная часть реагента, а к положительно поляризованному углероду – отрицательная часть реагента.
    СН2
+
= СН-
– СН+
= О-
+ Н+
: Br-
CH2
– CH = CH – OH CH2
– CH2
– CH = O СН2
+
= СН-
– СН+
= О-
+ Н+
: Br-
CH2
– CH = CH – OH CH2
– CH2
– CH = O
BrBr
3-бромпропаналь
Образующаяся при этом енольная форма альдегида немедленно превращается в более устойчивую карбонильную форму. Таким образом присоединение галогенводородов в радикал идет против правила Марковникова.
Ароматические альдегиды
Представители С6
Н5
–СН = О – бензойный альдегид. Это жидкость с запахом горького миндаля, содержится в косточках слив, вишен, диких абрикос и других плодах.
Список использованной литературы
1) Гранберг И.И. Органическая химия. - М., 2002
2) Ким А.М. Органическая химия. - Новосибирск, 2007
|