| Министерство образования и науки Российской Федерации
Федеральное агентство по образованию
Южно-Уральский государственный университет
Кафедра «Товароведение и экспертиза потребительских товаров»
КУРСОВАЯ РАБОТА
по дисциплине «Товароведение, экспертиза и стандартизация»
на тему «Изучение элементов химического состава пищевых продуктов (на примере белков)»
Выполнил:
Абидуллина Элеонора
Группа Ком-234
Проверил: Черкасова Эльвира Вячеславовна
Челябинск
2009 год
Содержание
| Введение……………………………………………………………………….
|
3
|
| 1. Литературный обзор
|
|
| 1.1. Общие понятия о белках
|
|
| 1.1.1. Химическая природа белков……………………………….....
|
4
|
| 1.1.2. Классификация белков………………………………………..
|
8
|
| 1.1.3. Свойства белков……………………………………………….
|
12
|
| 1.2. Влияние белков на организм человека…………………………….
|
14
|
| 1.3. Изменение содержания белков в процессе технологической обработки……………………………………………………………………...
|
17
|
| 1.4. Изменение содержания белков при хранении…………………….
|
20
|
| 2. Практическая часть
|
|
| 2.1. Характеристика количественных методов определения содержания белков…………………………………………………………….
|
21
|
| 2.2. Характеристика качественных методов определения содержания белков………………………………………………………………………….
|
25
|
| 3. Экспериментальная часть
|
|
| 3.1. Обоснование выбора объекта исследования……………………….
|
31
|
| 3.2. Анализ результатов собственных исследований…………………..
|
37
|
| Вывод…………………………………………………………………………...
|
40
|
| Список литературы……………………………………………………………
|
41
|
| Приложение……………………………………………………………………
|
42
|
Введение
Белки – это основной пластический материал для роста, развития и обновления организма. Они представляют собой основные структурные элементы всех тканей, входят в состав жидкой среды организма. Белки пищи расходуются на построение эритроцитов и гемоглобина, ферментов и гормонов, принимают активное участие в выработке защитных факторов – антител.
При недостаточном содержании белка в рационе в организме могут развиться тяжелые нарушения (гипотрофия, анемия, пр.), чаще возникают острые респираторные заболевания, которые принимают затяжное течение. Однако и избыток белка может отрицательно сказываться на здоровье. При длительном использовании высокобелковой пищи страдает функция почек и печени, повышается нервная возбудимость, часто появляются аллергические реакции, возможны интоксикации вследствие неполного распада и окисления белков с образованием токсических веществ.
Наиболее характерной причиной дисбаланса рационов питания является недостаточное потребление основных источников полноценного животного белка (мясо, рыба, молоко, яйца), растительных масел, свежих овощей и фруктов.
Поэтому изучение элементов химического состава пищевых продуктов, а в частности белков, является не просто важным, но и очень актуальным вопросом сегодня.
Целью работы является выявление важности белков для организма человека и основных источников белков.
В ходе данной работы ставятся следующие основные задачи: изучение химического состава белков, влияние их на организм человека, проблемы обработки и хранения белков, их свойства, изучение методов исследования содержания белков в пищевых продуктах, проверка соответствия фактического содержания белков в продукте нормируемому.
1. Литературный обзор
1.1. Общие понятия о белках
1.1.1. Химическая природа белков
Пептидная связь
Белки представляют собой нерегулярные полимеры, построенные из остатков аминокислот, общую формулу которых в водном растворе при значениях pH близких к нейтральным можно записать как NH3+CHRCOO – . Остатки аминокислот в белках соединены между собой амидной связью между амино- и карбоксильными группами. Пептидная связь между двумя аминокислотными остатками обычно называется пептидной связью, а полимеры, построенные из остатков аминокислот, соединенных пептидными связями, называют полипептидами. Белок как биологически значимая структура может представлять собой как один полипептид, так и несколько полипептидов, образующих в результате нековалентных взаимодействий единый комплекс.
Элементный состав белков
Изучая химический состав белков, необходимо выяснить, во-первых, из каких химических элементов они состоят, во-вторых, - строение их мономеров. Для ответа на первый вопрос определяют количественный и качественный состав химических элементов белка. Химический анализ показал наличие во всех белках углерода (50-55%), кислорода (21-23%), азота (15-17%), водорода (6-7%), серы (0,3-2,5%). В составе отдельных белков обнаружены также фосфор, йод, железо, медь и некоторые другие макро- и микроэлементы, в различных, часто очень малых количествах.
Содержание основных химических элементов в белках может различаться, за исключением азота, концентрация которого характеризуется наибольшим постоянством и в среднем составляет 16%. Кроме того, содержание азота в других органических веществах мало. В соответствии с этим было предложено определять количество белка по входящему в его состав азоту. Зная, что 1г азота содержится в 6,25 г белка, найденное количество азота умножают коэффициент 6,25 и получают количество белка.
Для определения химической природы мономеров белка необходимо решить две задачи: разделить белок на мономеры и выяснить их химический состав. Расщепление белка на его составные части достигается с помощью гидролиза – длительного кипячения белка с сильными минеральными кислотами (кислотный гидролиз) или основаниями (щелочной гидролиз). Наиболее часто применяется кипячение при 110 ° С с HCl в течение 24 ч. На следующем этапе разделяют вещества, входящие в состав гидролизата. Для этой цели применяют различные методы, чаще всего – хроматографию ( подробнее – глава “Методы исследования…”). Главным частью разделенных гидролизатов оказываются аминокислоты.
Аминокислоты
В настоящее время в различных объектах живой природы обнаружено до 200 различных аминокислот. В организме человека их, например, около 60. Однако в состав белков входят только 20 аминокислот, называемых иногда природными.
Аминокислоты – это органические кислоты, у которых атом водорода углеродного атома замещен на аминогруппу – NH2. Следовательно, по химической природе это аминокислоты с общей формулой:
R
|
H – C – NH2
|
COOH
Из этой формулы видно, что в состав всех аминокислот входят следующие общие группировки: – CH2, – NH2, – COOH. Боковые же цепи (радикалы – R ) аминокислот различаются. Химическая природа радикалов разнообразна: от атома водорода до циклических соединений. Именно радикалы определяют структурные и функциональные особенности аминокислот.
Все аминокислоты, кроме простейшей аминоуксусной к-ты глицина (NH3+CH2COO-) имеют хиральный атом Ca и могут существовать в виде двух энантиомеров (оптических изомеров): L-изомер и D-изомер.
Из двадцати основных аминокислот строятся белки, однако остальные, достаточно разнообразные аминокислоты образуются из этих 20 аминокислотных остатков уже в составе белковой молекулы. Среди таких превращений следует в первую очередь отметить образование дисульфидных мостиков при окислении двух остатков цистеина в составе уже сформированных пептидных цепей. В результате образуется из двух остатков цистеина остаток диаминодикарбоновой кислоты цистина. При этом возникает сшивка либо внутри одной полипептидной цепи, либо между двумя различными цепями. В качестве небольшого белка, имеющего две полипептидные цепи, соединенный дисульфидными мостиками, а также сшивки внутри одной из полипептидных цепей:
| |
GIVEQCCASVCSLYQLENYCN
| |
FVNQHLCGSHLVEALYLVCGERGFFYTPKA
Аминокислоты в водном растворе находятся в ионизированном состоянии за счет диссоциации амино- и карбоксильных групп, входящих в состав радикалов. Другими словами, они являются амфотерными соединениями и могут существовать либо как кислоты (доноры протонов), либо как основания (акцепторы доноров).
Все аминокислоты в зависимости от структуры разделены на несколько групп:
Ациклические
. Моноаминомонокарбоновые аминокислоты имеют в своем составе одну аминную и одну карбоксильную группы, в водном растворе они нейтральны. Некоторые из них имеют общие структурные особенности, что позволяет рассматривать их вместе:
1. Глицин и аланин. Глицин (гликокол или аминоуксусная к-та) является оптически неактивным – это единственная аминокислота, не имеющая энатиомеров. Глицин участвует в образовании нуклеиновых и желчных к-т, гема, необходим для обезвреживания в печени токсичных продуктов. Аланин используется организмом в различных процессах обмена углеводов и энергии. Его изомер b-аланин является составной частью витамина пантотеновой к-ты, коэнзима А (КоА), экстрактивных веществ мышц.
2. Серин и треонин. Они относятся к группе гидрооксикислот, т.к. имеют гидроксильную группу. Серин входит в состав различных ферментов, основного белка молока – казеина, а также в состав многих липопротеинов. Треонин участвует в биосинтезе белка, являясь незаменимой аминокислотой.
3. Цистеин и метионин. Аминокислоты, имеющие в составе атом серы. Значение цистеина определяется наличием в ее составе сульфгидрильной ( – SH) группы, которая придает ему способность легко окисляться и защищать организм о веществ с высокой окислительной способностью (при лучевом поражении, отравлении фосфором). Метионин характеризуется наличием легко подвижной метильной группы, использующейся для синтеза важных соединений в организме (холина, креатина, тимина, адреналина и др.)
4. Валин, лейцин и изолейцин. Представляют собой разветвленные аминокислоты, которые активно участвуют в обмене веществ и не синтезируются в организме.
Моноаминодикарбоновые аминокислоты имеют одну аминную и две карбоксильные группы и в водном растворе дают кислую реакцию. К ним относятся аспарагиновая и глутаминовая к-ты, аспарагин и глутамин. Они входят в состав тормозных медиаторов нервной системы.
Диаминомонокарбоновые аминокислоты в водном растворе имеют щелочную реакцию за сет наличия двух аминных групп. Относящийся к ним лизин необходим для синтеза гистонов а также в ряд ферментов. Аргинин участвует в синтезе мочевины, креатина.
Циклические.
Эти аминокислоты имеют в своем составе ароматическое или гетероциклическое ядро и, как правило, не синтезируется в организме человека и должны поступать с пищей. Они активно участвуют в разнообразных обменных процессах. Так фенил-аланин служит основным источником синтеза тирозина – предшественника ряда биологически важных веществ: гормонов (тироксина, адреналина), некоторых пигментов. Триптофан помимо участия в синтезе белка, служит компонентом витамина PP, серотонина, триптамина, ряда пигментов. Гистидин необходим для синтеза белков, является предшественником гистамина, влияющего на кровяное давление и секрецию желудочного сока.
1.1.2. Классификация белков
Все белки в зависимости от строения делятся на простые – протеины, состоящие только из аминокислот, и сложные - протеиды, имеющих небелковую протеистическую группу.
Протеины
Протеины представляют собой простые белки, состоящие только из белковой части. Они широко распространены в животном и растительном мире. К ним относятся альбумины и глобулины, встречающиеся практически во всех животных и растительных клетках, биологических жидкостях и выполняющих важные биологические функции. Альбумины участвуют в поддержании осмотического давления крови (создают онкотическое давление), транспортируют с кровью различные вещества. Глобулины входят в состав ферментов, составляющих основу иммуноглобулинов, выполняющих функции антител. В сыворотке крови между этими двумя компонентами существует постоянное соотношение – альбумино-глобулиновый коэффициент (А/Г), равный 1,7 – 2,3 и имеющий важное диагностическое значение.
Другими представителями протеинов являются протамины и гистоны – белки основного характера, содержащие много лизина и аргинина. Эти белки входят в состав нуклеопротеидов. Другой основной белок – коллаген – образует внеклеточное вещество соединительной ткани и находится в коже, хрящах и др. тканях.
Протеиды
Протеиды являются сложными белками, состоящими из белковой и небелковой частей. Название протеида определяется названием его простетической группы. Так, нуклеиновые кислоты являются небелковой частью нуклеопротеидов, фосфорная кислота входит в состав фосфопротеидов, углеводы – гликопротеидов, а липиды – липопротеидов.
Нуклеопротеиды.
Имеют важное значение, т.к. их небелковая часть представлена ДНК и РНК. Простетическая группа представлена в основном гистонами и протаминами. Такие комплексы ДНК с гистонами обнаружены в сперматозоидах, а с гистонами – в соматических клетках, где молекула ДНК “намотана” вокруг молекул гистонов. Нуклепротеидами по своей природе являются внеклеточные вирусы – это комплексы вирусной нуклеиновой кислоты и белковой оболочки – капсида.
Хромопротеиды.
Являются сложными белками, простетическая группа которых представлена окрашенными соединениями. К хромопротеидам относятся гемоглобин, миоглобин (белок мышц), ряд ферментов (каталаза, пероксидаза, цитохромы), а также хлорофилл.
Гемоглобин (Hb)
состоит из белка глобина и небелковой части гема, включающего атом Fe(II), соединенный с протопорфирином. Молекула гемоглобина состоит из 4-х субъединиц: двух a и двух b и соответственно содержит четыре полипептидные цепочки двух сортов. Каждая a-цепочка содержит 141, а b-цепочка – 146 аминокислотных остатков.
Миоглобин
. Хромопротеид, содержащийся в мышцах. Он состоит только из одной цепи, аналогичной субъединице гемоглобина. Миоглобин является дыхательным пигментом мышечной ткани. Он значительно легче гемоглобина связывается с кислородом, но труднее отдает его. Миоглобин создает запасы кислорода в мышцах, где его количество может достичь 14% всего кислорода организма. Это имеет важное значение, особенно для работы мышц сердца. Высокое содержание миоглобина обнаружено у морских млекопитающих (тюленя, моржа), что позволяет им длительное время находиться под водой.
Гликопротеиды
. Представляют собой сложные белки простетическая группа которых образована производными углеводов (аминосахарами, гексуроновыми кислотами). Гликопротеиды входят в состав клеточных мембран. Так, легочные стенки бактерий построены из пептидогликанов, являющихся производными линейных полисахаридов, несущих ковалентно связанные с ними пептидные фрагменты. Эти фрагменты осуществляют сшивание полисахаридных цепей с образованием механически прочной сетчатой структуры. Например, клеточная стенка E.coli построена из полисахаридных цепей, образованных остатками N-ацетилглюкозамина, связанными b-(1®4)связями, причем каждый второй остаток несет присоединенный к нему по атому С3 фрагмент, образованный связанными амидными связями остатками молочной кислоты, L-аланина, D-глутамата (через g-карбоксил), мезодиаминонимелината и D-аланина.
Гликопротеиды участвуют в транспорте различных веществ, в процессах свертывания крови, иммунитета, являются составными частями слизи и секретов желудочно-кишечного тракта. У арктических рыб гликопротеиды играют роль антифризов – веществ, препятствующих образованию кристаллов льда внутри их организма.
Фосфопротеиды
. Имеют в качестве небелкового компонента фосфорную к-ту. Представителями данных белков являются казеиноген молока, вителлин (белок желтков яиц), ихтулин (белок икры рыб). Такая локализация фосфопротеидов свидетельствует о важном их значении для развивающегося организма. У взрослых форм эти белки присутствуют в костной и нервной тканях.
Липопротеиды
. Сложные белки, простетическая группа которых образована липидами. По строению это небольшого размера (150-200 нм) сферические частицы, наружная оболочка которых образована белками (что позволяет им передвигаться по крови), а внутренняя часть – липидами и их производными. Основная функция липопротеидов – транспорт по крови липидов. В зависимости от количества белка и липидов, липопротеиды подразделяются на хиломикроны, липопротеиды низкой плотности (ЛПНП) и высокой плотности (ЛПВП), которые иногда обозначаются как a- и b-липопротеиды.
Хиломикроны
являются наиболее крупными из липопротеидов и содержат до 98-99% липидов и только 1-2% белка. Они образуются в слизистой оболочки кишечника и обеспечивают транспорт липидов из кишечника в лимфу, а затем в кровь.
1.1.3. Свойства белков
Белки имеют высокую молекулярную массу, некоторые растворимы в воде, способны к набуханию, характеризуются оптической активностью, подвижностью в электрическом поле и некоторыми другими свойствами.
Белки активно вступают в химические реакции
. Это свойство связано с тем, что аминокислоты, входящие в состав белков, содержат разные функциональные группы, способные реагировать с другими веществами. Важно, что такие взаимодействия происходят и внутри белковой молекулы, в результате чего образуется пептидная, водородная дисульфидная и другие виды связей. К радикалам аминокислот, а следовательно и белков, могут присоединяться различные соединения и ионы, что обеспечивает их транспорт по крови.
Белки являются высокомолекулярными соединениями
. Это полимеры, состоящие из сотен и тысяч аминокислотных остатков – мономеров. Соответственно и молекулярная масса белков находится в пределах 10 000 – 1 000 000. Так, в составе рибонуклеазы (фермента, расщепляющего РНК) содержится 124 аминокислотных остатка и ее молекулярная масса составляет примерно 14 000. Миоглобин (белок мышц), состоящий из 153 аминокислотных остатков, имеет молекулярную массу 17 000, а гемоглобин – 64 500 (574 аминокислотных остатка). Молекулярные массы других белков более высокие: g-глобулин ( образует антитела) состоит из 1250 аминокислот и имеет молекулярную массу около 150 000, а молекулярная масса фермента глутаматдегидрогеназы превышает 1 000 000.
Важнейшим свойством белков является их способность проявлять как кислые так и основные свойства, то есть выступать в роли амфотерных электролитов
. Это обеспечивается за счет различных диссоциирующих группировок, входящих в состав радикалов аминокислот. Например, кислотные свойства белку придают карбоксильные группы аспарагиновой глутаминовой аминокислоты, а щелочные – радикалы аргинина, лизина и гистидина. Чем больше дикарбоновых аминокислот содержится в белке, тем сильнее проявляются его кислотные свойства и наоборот.
Эти же группировки имеют и электрические заряды, формирующие общий заряд белковой молекулы
. В белках, где преобладают аспарагиновая и глутаминовая аминокислоты, заряд белка будет отрицательным, избыток основных аминокислот придает положительный заряд белковой молекуле. Вследствие этого в электрическом поле белки будут передвигаться к катоду или аноду в зависимости от величины их общего заряда. Так, в щелочной среде (рН 7 – 14) белок отдает протон и заряжается отрицательно, тогда как в кислой среде (рН 1 – 7) подавляется диссоциация кислотных групп и белок становится катионом.
Таким образом, фактором, определяющим поведение белка как катиона или аниона, является реакция среды, которая определяется концентрацией водородных ионов и выражается величиной рН. Однако при определенных значениях рН число положительных и отрицательных зарядов уравнивается и молекула становится электронейтральной, т.е. она не будет перемещаться в электрическом поле. Такое значение рН среды определяется как изоэлектрическая точка белков. При этом белок находится в наименее устойчивом состоянии и при незначительных изменениях рН в кислую или щелочную сторону легко выпадает в осадок. Для большинства природных белков изоэлектрическая точка находится в слабокислой среде (рН 4,8 – 5,4), что свидетельствует о преобладании в их составе дикарбоновых аминокислот.
Важное значение имеет способность белков адсорбировать
на своей поверхности некоторые вещества и ионы (гормоны, витамины, железо, медь), которые либо плохо растворимы в воде, либо являются токсичными (билирубин, свободные жирные кислоты). Белки транспортируют их по крови к местам дальнейших превращений или обезвреживания.
Водные растворы белков имеют свои особенности. Во-первых, белки обладают большим сродством к воде, т.е. они гидрофильны
. Это значит, что молекулы белка, как заряженные частицы, притягивают к себе диполи воды, которые располагаются вокруг белковой молекулы и образуют водную или гидратную оболочку. Эта оболочка предохраняет молекулы белка от склеивания и выпадения в осадок. Величина гидратной оболочки зависит от структуры белка. Например, альбумины более легко связываются с молекулами воды и имеют относительно большую водную оболочку, тогда как глобулины, фибриноген присоединяют воду хуже, и гидратная оболочка в них меньше. Таким образом, устойчивость водного раствора белка определяется двумя факторами: наличием заряда белковой молекулы и находящейся вокруг нее водной оболочки. При удалении этих факторов белок выпадает в осадок. Данный процесс может быть обратимым и необратимым.
Размер белковых молекул лежит в пределах 1 мкм до 1 нм и, следовательно, они являются коллоидными частицами
, которые в воде образуют коллоидные растворы. Эти растворы характеризуются высокой вязкостью, способностью рассеивать лучи видимого света, не проходят сквозь полупроницаемые мембраны.
1.2. Влияние белков на организм человека
Функции белков в организме разнообразны. Они в значительной мере обусловлены сложностью и разнообразием форм и состава самих белков. Белки содержатся во множестве продуктов, но основными источниками являются яйца, молоко и мясо (Таблица 1).
| |
животные белки
|
растительные белки
|
| среднее содержание белка
|
говядина
телятина
баранина
свинина
птица
продукты из свинины
рыба
выдержанные сыры
|
соя
пророщенные зерна пшеницы
морские водоросли
жареный арахис
чечевица
белая фасоль
миндаль
|
| высокое содержание белка
|
яйца
молоко
мягкие сыры
|
овсяные хлопья
хлеб с отрубями
шоколад с 70% содержанием какао
рожь
макаронные изделия из муки грубого помола
коричневый рис
грецкие орехи
|
Таблица 1 – Продукты, содержащие белки
Белки — незаменимый строительный материал. Одной из важнейших функций белковых молекул является пластическая
. Все клеточные мембраны содержат белок, роль которого здесь разнообразна. Количество белка в мембранах составляет более половины массы.
Многие белки обладают сократительной функцией
. Это, прежде всего, белки актин и миозин, входящие в мышечные волокна высших организмов. Мышечные волокна — миофибриллы — представляют собой длинные тонкие нити, состоящие из параллельных более тонких мышечных нитей, окруженных внутриклеточной жидкостью. В ней растворены аденозинтрифосфорная кислота (АТФ), необходимая для осуществления сокращения, гликоген — питательное вещество, неорганические соли и многие другие вещества, в частности кальций.
Велика роль белков в транспорте веществ
в организме. Имея различные функциональные группы и сложное строение макромолекулы, белки связывают и переносят с током крови многие соединения. Это, прежде всего, гемоглобин, переносящий кислород из легких к клеткам. В мышцах эту функцию берет на себя еще один транспортный белок — миоглобин.
Еще одна функция белка — запасная
. К запасным белкам относят ферритин — железо, овальбумин — белок яйца, казеин — белок молока, зеин — белок семян кукурузы.
Регуляторную функцию
выполняют белки-гормоны. Гормоны — биологически активные вещества, которые оказывают влияние на обмен веществ. Многие гормоны являются белками, полипептидами или отдельными аминокислотами. Одним из наиболее известных белков-гормонов является инсулин. Этот простой белок состоит только из аминокислот. Функциональная роль инсулина многопланова. Он снижает содержание сахара в крови, способствует синтезу гликогена в печени и мышцах, увеличивает образование жиров из углеводов, влияет на обмен фосфора, обогащает клетки калием.
Регуляторной функцией обладают белковые гормоны гипофиза — железы внутренней секреции, связанной с одним из отделов головного мозга. Он выделяет гормон роста, при отсутствии которого развивается карликовость. Этот гормон представляет собой белок с молекулярной массой от 27000 до 46000.
Одним из важных и интересных в химическом отношении гормонов является вазопрессин. Он подавляет мочеобразование и повышает кровяное давление. Вазопрессин — это октапептид циклического строения.
Регуляторную функцию выполняют и белки, содержащиеся в щитовидной железе — тиреоглобулины, молекулярная масса которых около 600000. Эти белки содержат в своем составе йод. При недоразвитии железы нарушается обмен веществ.
Другая функция белков — защитная
. На ее основе создана отрасль науки, названная иммунологией.
В последнее время в отдельную группу выделены белки с рецепторной функцией
. Есть рецепторы звуковые, вкусовые, световые и др.
Следует упомянуть и о существовании белковых веществ, тормозящих действие ферментов. Такие белки обладают ингибиторными функциями
. При взаимодействии с этими белками фермент образует комплекс и теряет свою активность, полностью или частично. Многие белки — ингибиторы ферментов — выделены в чистом виде и хорошо изучены. Их молекулярные массы колеблются в широких пределах; часто они относятся к сложным белкам — гликопротеидам, вторым компонентом которых является углевод.
Если белки классифицировать только по их функциям, то такую систематизацию нельзя было бы считать завершенной, так как новые исследования дают много фактов, позволяющих выделять новые группы белков с новыми функциями. Среди них уникальные вещества — нейропептиды
(ответственные за важнейшие жизненные процессы: сон, память, боль, чувство страха, тревоги).
1.3. Изменение содержания белков в процессе технологической обработки
Под действием обработки изменяются содержащиеся в продуктах белки, жиры, углеводы, витамины, минеральные и вкусовые вещества, что влияет на усваиваемость, пищевую ценность, массу, вкус, запах, цвет используемых продуктов.
Белки коагулируют
(свертываются) при температуре выше 70° С, теряют способность к набуханию, благодаря чему после тепловой обработки уменьшается масса мяса и рыбы.
Такие продукты, как мясо, рыба, яйца, нельзя перепаривать, так как при этом падает их усвояемость за счет изменений, происходящих в молекулах белка: коллаген переходит в глютин, размягчая ткани.
Денатурация белков -
это сложный процесс, при котором под влиянием внешних факторов (температуры, механического воздействия, действия кислот, щелочей, ультразвука и др.) происходит изменение вторичной, третичной и четвертичной структур белковой макромолекулы, т. е. нативной (естественной) пространственной структуры. Первичная структура, а следовательно, и химический состав белка не меняются. При кулинарной обработке денатурацию белков чаще всего вызывает нагревание. Процесс этот в глобулярных и фибриллярных белках происходит по-разному. В глобулярных белках при нагревании усиливается тепловое движение полипептидных цепей внутри глобулы, водородные связи, которые удерживали их в определенном положении, разрываются и полипептидная цепь развертывается, а затем сворачивается по-новому. При этом полярные (заряженные) гидрофильные группы, расположенные на поверхности глобулы и обеспечивающие ее заряд и устойчивость, перемещаются внутрь глобулы, а на поверхность ее выходят реакционноспособные гидрофобные группы (дисульфидные, сульфгидрильные и др.), не способные удерживать воду. Денатурация сопровождается изменениями важнейших свойств белка: потерей индивидуальных свойств (например, изменение окраски мяса при его нагревании вследствие денатурации миоглобина); потерей биологической активности (например, в картофеле, грибах, яблоках и ряде других растительных продуктов содержатся ферменты, вызывающие их потемнение, при денатурации белки-ферменты теряют активность); повышением атакуемости пищеварительными ферментами (как правило, подвергнутые тепловой обработке продукты, содержащие белки, перевариваются полнее и легче); потерей способности к гидратации (растворению, набуханию); потерей устойчивости белковых глобул, которая сопровождается их агрегированием (свертыванием, или коагуляцией, белка).
Агрегирование
- это взаимодействие денатурированных молекул белка, которое сопровождается образованием более крупных частиц. Внешне это выражается по-разному в зависимости от концентрации и коллоидного состояния белков в растворе. Так, в малоконцентрированных растворах (до 1%) свернувшийся белок образует хлопья (пена на поверхности бульонов). В более концентрированных белковых растворах (например, белки яиц) при денатурации образуется сплошной гель, удерживающий всю воду, содержащуюся в коллоидной системе.
Белки, представляющее собой более или менее обводненные гели (мышечные белки мяса, птицы, рыбы; белки круп, бобовых, муки после гидратации и др.), при денатурации уплотняются, при этом происходит их дегидратация с отделением жидкости в окружающую среду. Белковый гель, подвергнутый нагреванию, как правило, имеет меньшие объем, массу, большие механическую прочность и упругость по сравнению с исходным гелем нативных (натуральных) белков. Скорость агрегирования золей белка зависит от рН среды. Менее устойчивы белки вблизи изоэлектрической точки.
Деструкция белков
. При длительной тепловой обработке белки подвергаются более глубоким изменениям, связанным с разрушением их макромолекул. На первом этапе изменений от белковых молекул могут отщепляться функциональные группы с образованием таких летучих соединений, как аммиак, сероводород, фосфористый водород, углекислый газ и др. Накапливаясь в продукте, они участвуют в образовании вкуса и аромата готовой продукции. При дальнейшей гидротермической обработке белки гидролизуются, при этом первичная (пептидная) связь разрывается с образованием растворимых азотистых веществ небелкового характера (например, переход коллагена в глютин). Деструкция белков может быть целенаправленным приемом кулинарной обработки, способствующим интенсификации технологического процесса (использование ферментных препаратов для размягчения мяса, ослабления клейковины теста, получение белковых гидролизатов и др.).
Пенообразование
. Белки в качестве пенообразователей широко используют при производстве кондитерских изделий (тесто бисквитное, белково-взбивное), взбивании сливок, сметаны, яиц и др. Устойчивость пены зависит от природы белка, его концентрации, а также температуры.
1.4. Изменение содержания белков при хранении
При холодильном хранении и замораживании чистых растворов белков происходит агрегация молекул белка. Обычно этому процессу предшествует денатурация белка. Данные определения молекулярной массы, констант седиментации и скорости диффузии образующихся при замораживании и холодильном хранении белковых частиц свидетельствуют о структурных изменениях этого белка. По некоторым данным, в процессе холодильной обработки рыбы возможно не только понижение, но и повышение растворимости белка. Так, в балтийской сельди растворимость белка в мышечной ткани мороженой рыбы увеличивалась даже во время окоченения.
Во время хранения мяса создаются благоприятные условия для вторичного взаимодействия липидов с белками. Это происходит потому, что нативные белки при хранении быстро разрушаются, структурная упорядоченность клеточных мембран утрачивается, пространственная разграниченность химических компонентов клеток нарушается. Во взаимодействие с белками вступают при этом как полярные и нейтральные жиры, так и продукты их распада и окисления.
Взаимодействие между липидами и белками происходит в продуктах и при хранении в замороженном состоянии. Результаты исследования мяса и рыбы показали, что волнообразно изменялись растворимость различных белковых фракций мышечной ткани, содержание сульфгидрильных и дисульфидных групп в белках, а также активность ряда ферментов.
Качественный состав аминокислот в процессе хранения продукта определяется многими факторами и зависит от активности различных ферментов мышечной ткани и индивидуальные превращения аминокислот, от аминокислотного состава расщепляемых белков, их количества и степени атакуемости ферментами, изменении рН, температуры и других взаимосвязанных факторов.
2. Практическая часть
2.1. Характеристика количественных методов определения содержания белков
Методы количественного определения белковой фракции основаны на определении количества общего азота. Наиболее распространенным считают определение методом Кьельдаля, который позволяет выделять азот ввиде аммиака только из аминов и их производных, но некоторые азотсодержащие соединения в этих условиях наряду с аммиаком образуют также молекулярный азот, что приводит к получению заниженных данных.
Метод Кьельдаля.
Метод Кьельдаля относительно прост, хорошо воспроизводим, стандартизирован и имеет несколько модификаций.
Метод включает в себя три основных этапа: дигерирование, дистилляцию и титрование.
Метод основан на окислении органических веществ до СО2, Н2О, NH3 при нагревании с крепкой серной кислотой. Аммиак реагирует с избытком H2SO4 конц и образует с ней сульфат аммония.
R-CHNH2COOH + H2SO4 → CO2 + H2O + NH3;
2NH3 + H2SO4 → (NH4)2SO4.
После окончания сжигания навески избыток кислоты нейтрализуют щелочью, а аммиак, связанный в виде сульфата аммония, вытесняется избытком щелочи
(NH4)2SO4 + 2NaOH → Na2SO4 + 2NH4OH.
После сжигания навески определение азота ведется колориметрически по оптической плотности окрашенных растворов, полученных при взаимодействии с реактивом Несслера.
Аммиак и соли аммония способны образовывать с реактивом Несслера (двойная соль йодистой ртути и йодистого калия, растворенная в едком калии). Иодид меркураммония – вещество, окрашенное в желто-бурый цвет.
NH4OH + 2(HgI2KI) + 3KOH = OHg2NH2I + 7KI + 3H2O.
Исследование проводят по следующей схеме:
Навеску исследуемого продукта в объеме 0,04 г, взятую с точностью ±0,0001, помещают в пробирку. Затем последовательно вводят 2 мл H2SO4 (удельная плотность 1,84) и 1…2 капли H2O2 (33%). Проводят минерализацию, нагревая пробирку на водяной бане, при температуре 85 град.
Легко окисляющиеся вещества при этом полностью окисляются в течение 1…2 минуты, и обесцвеченная жидкость при дальнейшем нагревании остается бесцветной.
По окончании окисления, содержимое пробирки переводят количественно в мерную колбу на 100 мл до метки. Хорошо перемешав содержимое колбы, берут пробу в 10 мл и точно оттитровывают 0,5н NaOH по фенолфталеину, для определения количества щелочи, необходимой для нейтрализации.
После этого берут пробу того же раствора в 10 мл и переводят в другую мерную колбу на 100 мл, прибавляют установленное количество 0,5н NaOH для нейтрализации кислоты. После этого доводят водой до метки и хорошо взбалтывают. Эта жидкость используется для приготовления окрашенных растворов.
Приготовление окрашенных растворов. Для этого в двух мерных колбах емкостью по 100 мл готовят рабочий и стандартный растворы. В одну наливают 10 мл исследуемого раствора, доливают обе колбы на три четверти водой, после чего добавляют 4 мл раствора Несслера и доводят до метки.
Затем определяют оптическую плотность полученных окрашенных растворов.
На основании данных анализа проводят расчет содержания белка (%) по формуле:
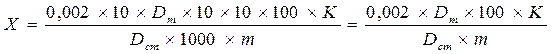 , ,
где 0,002 – количество мг азота в 1 мл стандартного рабочего раствора;
Dm - оптическая плотность рабочего раствора;
Dm – оптическая плотность стандартного раствора;
m – масса навески исследуемого вещества, г;
К – коэффициент пересчета азота на белок, равный для продуктов животного происхождения 6,25; для продуктов растительного происхождения 5,7.
Метод формольного титрования.
Другим количественным методом определения содержания белка является метод формольного титрования, который обычно применяют на молочных заводах.
Метод можно применять только для анализа свежего сырого молока кислотностью не выше 22 ºТ. Нельзя контролировать данным методом консервированные пробы.
Метод заключается в блокировке NH2-групп белков продукта внесенным формалином с образованием метилпроизводных белков, карбоксильные группы которых могут быть нейтрализованы щелочью:
HOOC – R – NH2 + 2HCHO → HCHO – R – N(CH2OH)2;
HCHO – R – N(CH2OH)2 + NaOH → NaOH – R – N(CH2OH)2 + H2O.
Количество щелочи, пошедшее на титрование кислых карбоксильных групп, пересчитывают на массовую долю белков.
Исследование проводят по следующей схеме:
В колбу вместительностью 100 см³ отмеривают 20 см³ исследуемого продукта, 10-12 капель 1% раствора фенолфталеина и титруют 0,1н раствором гидроксида натрия до появления розовой окраски, соответствующей цвету эталона. Затем вносят прибором для автоматического отмеривания 4 мл нейтрализованного 40% формалина и вновь титруют 0,1н раствором гидроксида натрия до окраски эталона. Количество щелочи, пошедшее на второе титрование (при первом титровании она расходуется на нейтрализацию веществ, обусловливающих кислотность продукта), умножают на коэффициент 0,959 и получают массовую долю белков в продукте в процентах.
Для перевода количества раствора гидроксида натрия в проценты белка можно пользоваться таблицей.
| Расход 0,1н раствора NaOH, мл
|
Массовая доля белка, %
|
Расход 0,1н раствора NaOH, мл
|
Массовая доля белка, %
|
| 2,45
|
2,35
|
3,15
|
3,03
|
| 2,50
|
2,40
|
3,20
|
3,07
|
| 2,55
|
2,44
|
3,25
|
3,12
|
| 2,60
|
2,49
|
3,30
|
3,16
|
| 2,65
|
2,54
|
3,35
|
3,21
|
| 2,70
|
2,59
|
3,40
|
3,25
|
| 2,75
|
2,64
|
3,45
|
3,31
|
| 2,80
|
2,69
|
3,50
|
3,35
|
| 2,85
|
2,73
|
3,55
|
3,40
|
| 2,90
|
2,78
|
3,60
|
3,45
|
| 2,95
|
2,83
|
3,65
|
3,50
|
| 3,00
|
2,88
|
3,70
|
3,55
|
| 3,05
|
2,93
|
3,75
|
3,60
|
| 3,10
|
2,98
|
3,80
|
3,65
|
Таблица 2 - Зависимость массовой доли белков от объема раствора щелочи, затраченного на титрование проб в присутствии формалина
2.2. Характеристика качественных методов определения содержания белков
Реакции осаждения белков
Белки в растворе и соответственно в организме сохраняются в нативном состоянии за счет факторов устойчивости, к которым относятся заряд белковой молекулы и гидратная оболочка вокруг нее. Удаление этих факторов приводит к склеиванию молекул белков и выпадению их в осадок. Осаждение белков может быть обратимым и необратимым в зависимости от реактивов и условий реакции. В лабораторной практике реакции осаждения используют для выделения альбуминовой и глобулиновой фракций белков, количественной характеристики их устойчивости, обнаружения белков в биологических жидкостях и освобождения от них с целью получения без белкового раствора.
Обратимое осаждение.
Под действием факторов осаждения белки выпадают в осадок, но после прекращения действия (удаления) этих факторов белки вновь переходят в растворимое состояние и приобретают свои нативные свойства. Одним из видов обратимого осаждения белков является высаливание.
Высаливание
. Насыщенным раствором сульфата аммония осаждается альбуминовая фракция белков, полунасыщенным раствором - глобулиновая фракция.
Сущность реакции заключается в дегидратации молекул белка.
Ход определения. В пробирку наливают 30 капель неразведенной пробы и добавляют равное количество насыщенного раствора сульфата аммония. Содержимое пробирки перемешивают. Получают полунасыщенный раствор сульфата аммония, при этом глобулиновая фракция осаждается, а альбуминовая остается в растворе. Последнюю отфильтровывают, затем смешивают с порошком сульфата аммония до тех пор пока не прекратится растворение соли, при этом выпадает осадок - глобулины.
Необратимое осаждение белков.
Необратимое осаждение белков связано с глубокими нарушениями структуры белков (вторичной и третичной) и потерей ими нативных свойств. Такие изменения белков можно вызвать кипячением, действием концентрированных растворов минеральных и органических кислот, солями тяжелых металлов.
Осаждение при кипячении
. Белки являются термолабильными соединениями и при нагревании свыше 50-60 градусов С денатурируются. Сущность тепловой денатурации заключается в разрушении гидратной оболочки, разрыве стабилизирующих белковую глобулу связей и развертывании белковой молекулы. Наиболее полное и быстрое осаждение происходит в изоэлектрической точке (когда заряд молекулы равен нулю), поскольку частицы белка при этом наименее устойчивы. Белки, обладающие кислыми свойствами, осаждаются в слабокислой среде, а белки с основными свойствами - в слабощелочной. В сильнокислых или сильнощелочных растворах денатурированный при нагревании белок в осадок не выпадает, так как его частицы перезаряжаются и несут в первом случае положительный, а во втором - отрицательный заряд, что повышает их устойчивость в растворе.
Ход определения. В 4 пронумерованные пробирки приливают по 10 капель раствора пробы. Затем 1-ю пробирку нагревают до кипячения, при этом раствор мутнеет, но так как частицы денатурированного белка несут заряд, они в осадок не выпадают. Это связано с тем, что яичный белок имеет кислые свойства (его изоэлектрическая точка 4,8) и в нейтральной среде заряжен отрицательно; во вторую пробирку добавляют 1 каплю 1% раствора уксусной кислоты и нагревают до кипячения. Белок выпадает в осадок, т.к. его раствор приближается к изоэлектрической точке и белок теряет заряд (один из факторов устойчивости белка в растворе); в 3-ю пробирку добавляют 1 каплю 10% раствора уксусной кислоты и нагревают до кипения. Осадка не образуется, так как в сильнокислой среде частицы белка приобретают положительный заряд (сохраняется один из факторов устойчивости белка в растворе); в 4-ю пробирку наливают 1 каплю раствора NaOH, нагревают до кипения. Осадок не образуется, поскольку в щелочной среде отрицательный заряд белка увеличивается.
Осаждение концентрированными минеральными кислотами.
Концентрированные кислоты (серная, хлористоводородная, азотная и др.) вызывают денатурацию белка за счет удаления факторов устойчивости белка в растворе (заряда и гидратной оболочки). Однако при избытке хлористоводородной и серной кислоты выпавший осадок денатурированного белка снова растворяется. По-видимому, это происходит в результате перезарядки молекул белка и частичного их гидролиза. При добавлении избытка азотной кислоты растворения осадка не происходит. Вот почему для определения малых количеств белка в моче при клинических исследованиях применяется азотная кислота.
Ход определения. В три пробирки наливают по 5 капель концентрированной серной, хлористоводородной и азотной кислот. Затем, наклонив пробирку под углом 45 градусов, осторожно по стенке наслаивают такой же объем пробы. На границе двух слоев появляется осадок белка в виде белого кольца. Осторожно встряхивают пробирки, наблюдают растворение белка в пробирках с серной и хлористоводородной кислотами, в пробирке с азотной кислотой растворения белка не происходит.
Осаждение органическими кислотами
. Трихлоруксусная кислота осаждает только белки, а сульфосалициловая осаждает не только белки, но и высокомолекулярные пептиды.
Ход определения. В две пробирки вносят по 5 капель раствора пробы. В одну из них прибавляют 2 капли сульфосалициловой кислоты, а в другую - 5 капель трихлоруксусной кислоты. В пробирках выпадает осадок белка.
Осаждение белка солями тяжелых металлов.
Белки при взаимодействии с солями свинца, меди, ртути, серебра и других тяжелых металлов денатурируются и выпадают в осадок. Однако при избытке некоторых солей наблюдается растворение первоначально образовавшегося осадка. Это связано с накоплением ионов металла на поверхности денатурированного белка и появлением положительного заряда на белковой молекуле.
Ход определения. В три пробирки вносят по 5 капель пробы. В первую добавляют 1 каплю ацетата свинца, в третью - 1 каплю нитрата серебра. Во всех пробирках выпадает осадок. Затем в первую пробирку добавляют 10 капель нитрата серебра - растворения осадка нет.
Цветные реакции на белки
Цветные реакции применяются для установления белковой природы веществ, идентификации белков и определение их аминокислотного состава в различных биологических жидкостях.
Биуретовая реакция на пептидную связь.
В основе ее лежит способность пептидных связей (-CO-NH-) образовывать с сульфатом меди в щелочной среде окрашенные комплексные соединения, интенсивность окраски которых зависит от длины полипептидной цепи. Раствор белка дает сине-фиолетовое окрашивание.
Ход определения. В пробирку вносят 5 капель раствора пробы, 3 капли NaOH, 1 каплю Cu(OH)2, перемешивают. Содержимое пробирки приобретает сине-фиолетовое окрашивание.
Нингидриновая реакция
. Сущность реакции состоит в образовании соединения, окрашенного в сине-фиолетовый цвет, состоящего из нингидрина и продуктов гидролиза аминокислот. Эта реакция характерна для аминогрупп в -положении, присутствующих в природных аминокислотах и белках.
Ход определения. В пробирку вносят 5 капель раствора пробы, затем 5 капель нингидрина, нагревают смесь до кипения. Появляется розово-фиолетовое окрашивание, переходящее с течением времени в сине-фиолетовое.
Ксантопротеиновая реакция
. При добавлении к раствору белка концентрированной азотной кислоты и нагревании появляется желтое окрашивание, переходящее в присутствии щелочи в оранжевое. Сущность реакции состоит в нитровании бензольного кольца циклических аминокислот азотной кислотой с образованием нитросоединений, выпадающих в осадок. Реакция выявляет наличие в белке циклических аминокислот.
Ход определения. К 5 каплям раствора пробы добавляют 3 капли азотной кислоты и (осторожно!) нагревают. Появляется осадок желтого цвета. После охлаждения добавляют (желательно на осадок) 10 капель NaOH, появляется оранжевое окрашивание.
Реакция Адамкевича
. Аминокислота триптофан в кислой среде, взаимодействуя с альдегидами кислот, образует продукты конденсации красно-фиолетового цвета.
Ход определения. К одной капле пробы прибавляют 10 капель уксусной кислоты. Наклонив пробирку, осторожно по стенке добавляют по каплям 0,5 мл серной кислоты так, чтобы жидкости не смешивались. При стоянии пробирки на границе жидкостей появляется красно-фиолетовое кольцо.
Реакция Фоля
. Аминокислоты, содержащие сульфгидрильные группы - SH, подвергаются щелочному гидролизу с образованием сульфида натрия Na2S. Последний, взаимодействуя с плюмбитом натрия (образуется в ходе реакции между ацетатом свинца и NaOH), образует осадок сульфида свинца PbS черного или бурого цвета.
Ход определения. К 5 каплям раствора пробы прибавляют 5 капель реактива Фоля ( к 5% раствору ацетата свинца прибавляют равный объем 30% раствора NaOH до растворения образовавшегося осадка). и кипятят 2-3 мин. После отстаивания 1-2 мин. появляется черный или бурый осадок.
3. Эксперементальная часть
3.1. Обоснование выбора объекта исследования
Я выбрала в качестве объекта своего исследования яйцо куриное, так как оно является основным источником белка и многих необходимых для организма человека веществ, и яйцо входит в рацион питания каждого человека.
Ежегодно в мире потребляется около биллиона, то есть тысячи миллиардов яиц. Каждый человек съедает в среднем около 200 яиц в год. Но яйца - это не просто обычный продукт питания.
В яйцах содержится не только богатый коктейль питательных веществ, благодаря яйцам ваша кулинарная фантазия не будет иметь границ. В Германии на завтрак любят яйца всмятку, американцы именуют свою яичницу "sunny side up" - "солнечной стороной кверху", испанцы влюблены в свою тортилью, итальянцы предпочитают фритату - разновидность омлета, а японцы-гурманы окунают сырое мясо в только что снесенные яйца.
Пожалуй, ни один другой продукт не используется на кухне так часто, как свежее яйцо. В пирогах, десертах, мороженом, изысканных соусах или всеми любимых яичных макаронах - всюду яйца выдают себя золотистым цветом желтка.
Высочайшее качество белка и комбинация различных жизненно важных элементов делают яйца чрезвычайно ценным продуктом питания. Яйцо крупного размера содержит примерно девять граммов белка, восемь граммов жиров, ценный элемент лецитин, а также другие минеральные вещества и витамины - за исключением витамина С. Витамины скрываются, в основном, в желтке.
Самым важным витамином является витамин А и его провитамины - каротиноиды. Так называемый "глазной витамин" улучшает зрение. Он необходим в сетчатке глаза как для восприятия света и темноты, так и для различения цвета. Витамин А играет также важную роль в иммунной системе, способствуя росту и укреплению волос, кожи и зубов.
Куриные яйца являются также источником витамина В, отвечающего за бесперебойный обмен веществ, дыхание клеток и образование красных кровяных телец - эритроцитов.
Одно яйцо покрывает дневную потребность человека в фолиевой кислоте на 26 процентов. Этот особо неустойчивый витамин создает новые клетки и активирует рост. Недостаток фолиевой кислоты является одной из самых распространенных форм дефицита витаминов и зачастую проявляется вместе с недостатком железа. Но яйца являются и настоящей кладовой минеральных веществ: кальций, магнезий, калий, железо, цинк, йод и фтор делают яйцо одним из самых питательных продуктов на Земле.
Яйца - хороший источник белка, поэтому в приведенной ниже таблице, они используются как основа для сравнения с другими продуктами. Яйцам присвоена условная ценность 100.
| Продукт
|
Белковый рейтинг
|
| Яйца (в целом)
|
100
|
| Рыба
|
70
|
| Говядина постная
|
69
|
| Молоко коровье
|
60
|
| Рис бурый
|
57
|
| Рис светлый
|
56
|
| Соевые бобы
|
47
|
| Пшено цельное
|
44
|
| Арахис
|
43
|
| Бобы сушенные
|
34
|
| Картошка
|
34
|
Таблица 3 – Рейтинг пищевых продуктов, содержащих белки
В приведенных данных речь идет о яйцах в целом, а не о белках или желтках. В наши дни модно употреблять в пищу только белки, так как они не содержат жир. На самом деле в желтках содержание белка не меньше. А содержание витаминов и минералов даже больше.
На основании данных таблицы можно сделать вывод, что яйца – это основной источник белков.
Куриное яйцо по сравнению с другими животными продуктами содержит самый полноценный белок, практически полностью усваивающийся организмом. Белок яйца содержит в наиболее оптимальных соотношениях все незаменимые аминокислоты.
Яйца содержат полный белок, то есть в этих продуктах находятся все аминокислоты, для того чтобы организм выработал полезный белок. В различных продуктах содержатся разные количества на единицу веса полезного белка.
Ниже приведена таблица, в которой показано весовое содержание белка в некоторых продуктах - поставщиках белка и процент этого белка, который фактически может быть усвоен нашим организмом.
| Продукт
|
Весовой процент белка
|
Процент усваемого белка
|
| Яйцо
|
12
|
94
|
| Молоко
|
4
|
82
|
| Рыба
|
18-25
|
80
|
| Сыр
|
22-36
|
70
|
| Бурый рис
|
8
|
70
|
| Мясо, птица
|
19-31
|
68
|
| Мука соевая
|
42
|
61
|
Таблица 4 – весовое содержание белка в продуктах, %
Из таблицы видно, что, к примеру, яйца содержат лишь 12% белка, но благодаря определенному составу аминокислот 94% белка может быть усвоено организмом. С другой стороны, белок составляет 42% соевой муки, но состав этого белка позволяет усвоить лишь 61% этого количества.
На основании данных таблицы можно сделать вывод, что существует огромное различие между общим содержание белка в продуктах (то, которое мы читаем на этикетках) и тем количеством, которое организм фактически использует.
Если посмотреть на список в таблице, то можно отметить, что такие продукты, как рис, бобы и картошка, содержат намного меньше полезного белка, чем яйца. Причина этого в слишком малом содержании нужных аминокислот, необходимых для полного усвоения белка организмом.
Соответственно, белки, в которых не хватает заменимых аминокислот, называются неполноценными; те же, в которых незаменимых аминокислот достаточно – полноценными, белки яиц полноценны.
Таким образом, можно сделать вывод, что куриное яйцо по сравнению с другими животными продуктами содержит самый полноценный белок, практически полностью усваивающийся организмом. Белок яйца содержит в наиболее оптимальных соотношениях все незаменимые аминокислоты.
По действующим российским стандартам маркировка должна быть на каждом яйце, произведенном на птицефабрике.
Первый знак в маркировке означает допустимый срок хранения:
Буква "Д" - обозначает диетическое яйцо, такие яйца реализуются в течение 7 дней.
Буква "С" - обозначает столовое яйцо, которое реализуется в течение 25 дней.
Второй знак в маркировке означает категорию яйца в зависимости от его веса:
Яйцо с двумя желтками Третья категория (3) - от 35 до 44,9 г.
Вторая категория (2) - от 45 до 54,9 г.
Первая категория (1) - от 55 до 64,9 г.
Отборное яйцо (О) - от 65 до 74,9 г.
Высшая категория (В) - 75 г и более.
Характеристика объекта исследования
В качестве объекта исследования я выбрала три образца – яйца куриные, произведенные на ОАО «Птицефабрика Челябинская» (ЧЕПФА).
ОАО «Птицефабрика Челябинская» входит в пятерку крупнейших птицеводческих предприятий России. Основным направлением деятельности является производство, переработка, хранение и реализация сельскохозяйственной продукции. Основная продукция птицефабрики - высококачественное куриное яйцо, полученное от птицы кросса «ломанн ЛСЛ-классик». Сегодня ОАО «Птицефабрика Челябинская» объединяет пять структурных подразделений: птицефабрика Челябинская, Еманжелинский племрепродуктор, Петропавловский зерновой комплекс, Еманжелинский хлебоприёмный пункт и санаторий «Курочкино».
Образец №1 - яйцо диетическое первой категории (Д1), произведенное 26 марта 2009 года, имеющее массу 62 грамма.
Образец №2 - яйцо столовое первой категории (С1), произведенное 26 марта 2009 года, имеющее массу 59 грамм.
Образец №3 – яйцо столовое отборное (СО), произведенное 26 марта 2009 года, имеющее массу 68 грамм.
Метод оценки содержания белка
В рамках работы использовался в качестве метода оценки содержания белка в продукте микрометод Кьельдаля-Голуба.
Исследование проводят по следующей схеме:
Навеску исследуемого продукта в объеме 0,04 г, взятую с точностью ±0,0001, помещают в пробирку. Затем последовательно вводят 2 мл H2SO4 (удельная плотность 1,84) и 1…2 капли H2O2 (33%). Проводят минерализацию, нагревая пробирку на водяной бане, при температуре 85 град.
Легко окисляющиеся вещества при этом полностью окисляются в течение 1…2 минуты, и обесцвеченная жидкость при дальнейшем нагревании остается бесцветной.
По окончании окисления, содержимое пробирки переводят количественно в мерную колбу на 100 мл до метки. Хорошо перемешав содержимое колбы, берут пробу в 10 мл и точно оттитровывают 0,5н NaOH по фенолфталеину, для определения количества щелочи, необходимой для нейтрализации.
После этого берут пробу того же раствора в 10 мл и переводят в другую мерную колбу на 100 мл, прибавляют установленное количество 0,5н NaOH для нейтрализации кислоты. После этого доводят водой до метки и хорошо взбалтывают. Эта жидкость используется для приготовления окрашенных растворов.
Приготовление окрашенных растворов. Для этого в двух мерных колбах емкостью по 100 мл готовят рабочий и стандартный растворы. В одну наливают 10 мл исследуемого раствора, доливают обе колбы на три четверти водой, после чего добавляют 4 мл раствора Несслера и доводят до метки.
Затем определяют оптическую плотность полученных окрашенных растворов.
На основании данных анализа проводят расчет содержания белка (%) по формуле:
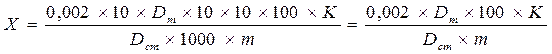 , ,
где 0,002 – количество мг азота в 1 мл стандартного рабочего раствора;
Dm - оптическая плотность рабочего раствора;
Dm – оптическая плотность стандартного раствора;
m – масса навески исследуемого вещества, г;
К – коэффициент пересчета азота на белок, равный для продуктов животного происхождения 6,25; для продуктов растительного происхождения 5,7.
3.2. Анализ результатов собственных исследований
Данные содержания белка в образцах наглядно представлены на накопительной диаграмме (рисунок 21), где отражены вклад каждого показателя в комплексное содержание белка в образцах и общее процентное количество для каждого из них.
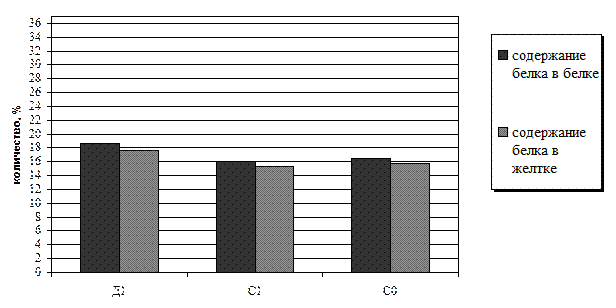
Рисунок 1 – Содержание белка в исследуемых образцах
| Образец
|
Количество содержания белка в белке яйца, %
|
Количество содержания в желтке яйца, %
|
| Яйцо диетическое (Д1)
|
18,7
|
17,6
|
| Яйцо столовое первой категории (С1)
|
16,1
|
15,3
|
| Яйцо столовое отборное (СО)
|
16,5
|
15,7
|
Таблица 5 – Количество содержания белка в исследуемых образцах
Больше всего белка содержится в диетическом яйце первой категории (Д1) (Образец №1). Это объясняется тем, что диетическое яйцо - самое свежее яйцо, снесенное не более недели назад. По данным исследований на протяжении недели в яйце продолжают происходить микробиологические процессы, т.е. оно живет. За неделю хранения качественный и количественный состав белка и аминокислот в яйцах не успевает сильно измениться. Но в соответствии с литературными данными в яичном белке диетического яйца белка должно содержаться около 19% белка, а в желтке около 18%, а в ходе исследования выявилось, что в белке содержание белка составляет 18,7%, а в желтке 17,6%. Можно сделать вывод, что отклонения содержания белка небольшие, но все же есть, что объясняется неправильным хранением яйца.
В яйце столовом отборном (СО) (Образец №3) белка содержится меньше, чем диетическом яйце, что объясняется сроком хранения яйца. Яйцо небходимо хранить в холодном, но не слишком сухом месте; наилучшая температура 0 — +5 °С. Если поддерживать оптимальную влажность воздуха и содержание в нем углекислого газа, можно хранить яйца до 9 месяцев. Но при этом происходит денатурация и агрегирование белка в яйце. В соответствии с литературными данными в яичном белке столового яйца белка должно содержаться около 17% белка, а в желтке около 16%, а в ходе исследования выявилось, что в белке содержание белка составляет 16,5%, а в желтке 15,7%. Можно сделать вывод, что отклонения содержания белка небольшие, но все же есть, что объясняется тем, что при хранении не соблюдаются все необходимые условия.
В яйце столовом первой категории (С1) (Оразец №2) содержание белка несильно отличается от содержания белка в яйце столовом отборном, что объясняется тем, что яйцо столовое первой категории отличается от яйца столового отборного только массой. В белке Образца №2 содержание белка составляет 16,5%, а в желтке 15,7%, что соответствует литературным данным, но с некоторыми отклонениями.
Вывод
В ходе данной работы было выявлено, что белки — это органические вещества животного или растительного происхождения, которые обеспечивают поддержку клеточной структуры человеческого организма. Их основным элементом являются многочисленные аминокислоты.
Аминокислоты содержатся во всех продуктах растительного и животного происхождения, однако содержание и соотношение их в продуктах разное.
Объектом исследования стало куриное яйцо как основной источник белков. На основании результатов исследования можно сделать вывод, что качество яиц современных производителей и содержание в них белка соответствует нормируемым показателям, но с небольшими отклонениями, что объясняется длительностью хранения и возможным несоответствием режима хранения яиц.
В ходе работы была достигнута главная цель: выявлены основные источники белков – это продукты животного происхождения — молоко, мясо, рыба, яйца (содержат незаменимые аминокислоты в наиболее благоприятных соотношениях) и растительного происхождения, как горох, фасоль, гречневая и перловая крупы, пшено, рис; а также определено то, что белки – это необходимые и жизненноважные элементы химического состава пищевых продуктов, которые выполняют много функций – пластическая, сократительная, запасная, регуляторная и защитная.
Белки – это основа здорового и правильного питания, поэтому необходимо повышать культуру питания населения страны и пропагандировать здоровый образ жизни.
Список литературы
1. Потороко И.Ю., Калинина И.В. Теоретические основы товароведения и экспертизы потребительских товаров: Лабораторный практикум. – Челябинск: Изд-во ЮУрГУ, 2005. – 97 с.
2. Товароведение мясных и яичных товаров. Товароведение молочных товаров и пищевых концентратов: Учеб./Г. Н. Кругляков, Г. В. Круглякова.-М.:Маркетинг,2001.
3. Химический состав российских пищевых продуктов/Под ред. И. М. Скурихина, В. А. Тутельяна; Рос. акад. мед. наук, Ин-т питания.-М.:ДеЛи принт,2002.
4. http://ru.wikipedia.org/wiki/Белки
5. http://www.chepfa.ru
Приложение 1
Дневник расчетов
Образец №1. Яйцо диетическое первой категории
Белок
: оптическая плотность исследуемого образца – 0,237
оптическая плотность стандартного раствора – 0,35
масса навески – 0,0465 г
Х=(0,002х0,237х100х6,25)/(0,35х0,0465)=18,1%
Желток:
оптическая плотность исследуемого образца – 0,220
оптическая плотность стандартного раствора – 0,35
масса навески – 0,0457 г
Х=(0,002х0,220х100х6,25)/(0,35х0,0457)=17,3%
Образец №2. Яйцо столовое первой категории
Белок
: оптическая плотность исследуемого образца – 0,186
оптическая плотность стандартного раствора – 0,35
масса навески – 0,0401 г
Х=(0,002х0,186х100х6,25)/(0,35х0,0401)=16,5%
Желток
: оптическая плотность исследуемого образца – 0,179
оптическая плотность стандартного раствора – 0,35
масса навески – 0,0406 г
Х=(0,002х0,179х100х6,25)/(0,35х0,0406)=15,7%
Образец №3. Яйцо столовое отборное
Белок
: оптическая плотность исследуемого образца – 0,179
оптическая плотность стандартного раствора – 0,35
масса навески – 0,0443 г
Х=(0,002х0,179х100х6,25)/(0,35х0,0443)=16,1%
Желток
: оптическая плотность исследуемого образца – 0,176
оптическая плотность стандартного раствора – 0,35
масса навески – 0,0409 г
Х=(0,002х0,176х100х6,25)/(0,35х0,0409)=15,3%
|